ДНК-роботы — это нано (100 нм) устройства, созданные с использованием ДНК как основного строительного материала. Эти роботы могут выполнять определенные задачи на молекулярном уровне и имеют потенциал революционизировать медицину.

ДНК (дезоксирибонуклеиновая кислота) — это длинная молекула, содержащая генетическую информацию, необходимую для развития, функционирования, роста и размножения всех известных живых организмов и многих вирусов.
ДНК-наноробот, разумеется, состоит не из железок, как можно представить по названию. Это химические молекулы, которыми можно управлять и доставлять к нужному месту в организме. ДНК обладает способностью формировать сложные трехмерные структуры благодаря комплементарному спариванию оснований, что позволяет создавать точные и программируемые формы и устройства.
Описание
ДНК-роботы могут быть запрограммированы для выполнения различных задач, таких как доставка лекарств, диагностика заболеваний, сбор и анализ биологических молекул, и даже вмешательство в клеточные процессы.
Каждый наноробот выполнен из плоского, прямоугольного листа ДНК-оригами, размером 90 на 60 нанометров. К поверхности прикрепляется ключевой кровянистый фермент, называемый тромбином. Тромбин может блокировать кровоток в опухоли путем свертывания крови в сосудах, которые питают рост опухоли, вызывая у опухоли своего рода мини-сердечный приступ и приводя к гибели опухолевой ткани.
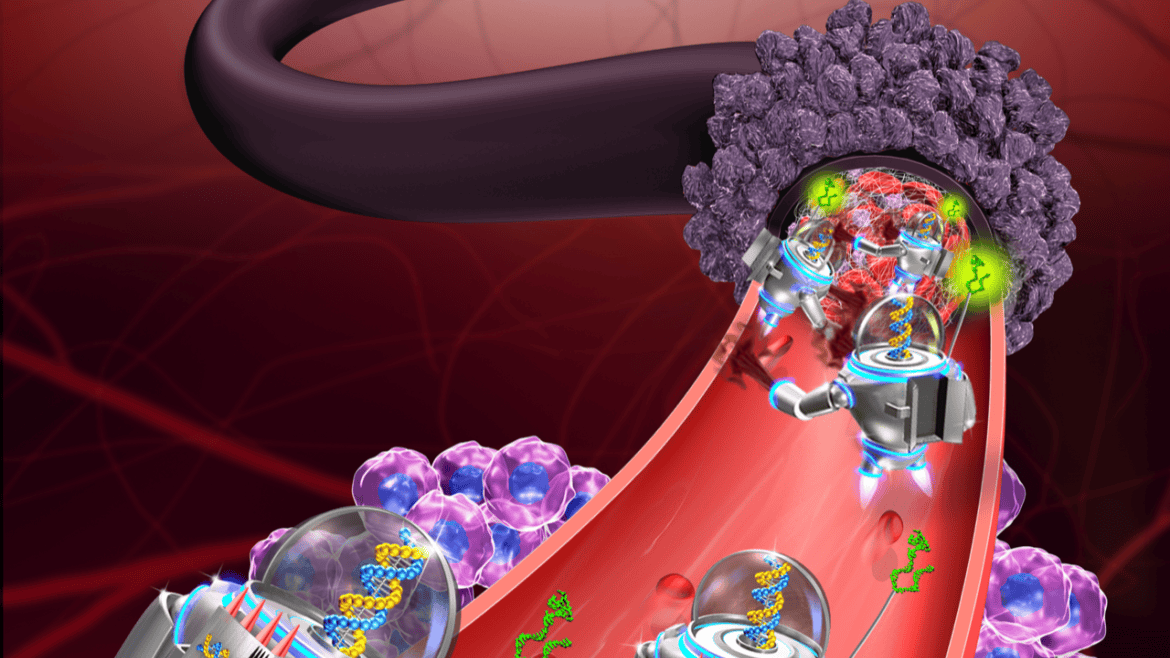
Ключ к программированию наноробота, который атакует только раковую клетку, включает специальную полезную нагрузку на поверхности, называемую аптамером ДНК. Аптамер ДНК может специфически нацеливаться на белок, называемый нуклеолин (ядрышковый белок), который производится в больших количествах только на поверхности эндотелиальных клеток опухоли и не находится на поверхности здоровых клеток.
Основные функциями такого робота включают:
- Таргетная доставка лекарств: ДНК-роботы могут быть использованы для доставки лекарств непосредственно к пораженным клеткам или тканям, минимизируя побочные эффекты и повышая эффективность лечения.
- Диагностика: Они могут служить в качестве высокочувствительных сенсоров для обнаружения биомаркеров заболеваний на ранних стадиях.
- Ремонт клеток: Потенциально ДНК-роботы могут вмешиваться в клеточные процессы для восстановления или замены поврежденных молекул или клеток.
Реализация ДНК роботов
Существует несколько методов синтеза ДНК, основной это Машины для синтеза ДНК. Автоматизированные устройства, которые могут синтезировать длинные цепи ДНК.
После синтеза отдельных фрагментов ДНК их необходимо объединить в более длинные последовательности. Это может быть сделано с помощью различных методов клонирования и сборки
Синтетическая ДНК затем вводится в живую клетку, чтобы она могла начать функционировать.
Преимущества проекта
Исследования, упомянутые в статье CORDIS, показывают, что ДНК-нанороботы могут существенно изменить подходы к лечению и диагностике заболеваний, делая их более точными и эффективными. Например, они могут быть использованы для целенаправленного воздействия на раковые клетки или для лечения вирусных инфекций путем точного вмешательства на молекулярном уровне.
Использование ДНК как строительного материала также обеспечивает биосовместимость и минимальную токсичность, что делает эти нанороботы потенциально безопасными для применения в живых организмах.
Несмотря на перспективность и потенциал ДНК-роботов, существуют некоторые недостатки и вызовы, которые необходимо учитывать:
- Разрушение в организме: ДНК-роботы могут быть подвержены разрушению ферментами (например, нуклеазами) в организме, что ограничивает их стабильность и долговечность.
- Риск иммунной реакции: Введение ДНК-роботов в организм может вызвать иммунный ответ, что может привести к воспалению или другим нежелательным
Для преодоления этих недостатков необходимы дальнейшие исследования и разработки. Несмотря на текущие вызовы, прогресс в области нанотехнологий и молекулярной биологии дает основания для оптимизма в отношении будущих улучшений и возможностей использования ДНК-роботов в медицине.
Заключение
ДНК-роботы представляют собой революционную технологию с огромным потенциалом для медицины, особенно в области таргетной доставки лекарств и диагностики. Несмотря на значительные преимущества, они сталкиваются с рядом вызовов, таких как стабильность, иммунные реакции и сложности производства. Эти проблемы требуют дальнейших исследований и технологических усовершенствований. Тем не менее, перспективы улучшения и адаптации ДНК-роботов для клинического применения внушают оптимизм. В долгосрочной перспективе, успешное преодоление существующих недостатков может привести к значительным прорывам в лечении и диагностике множества заболеваний.